2HI + Pb(OH)2 = Pbl2v + 2Н2O
Металлы и амфигены, стоящие в ряду напряжений левее водорода и не реагирующие с водой, вступают во взаимодействие с сильными кислотами НCl, НВr и HI (в общем виде НГ) в разбавленном растворе и вытесняют из них водород (приведены реально протекающие реакции):
М + 2НГ = МГ2 + Н2^ (М = Be, Mg, Zn, Cr, Mn, Fe, Co, Ni)
2M + 6НГ = 2МГ3 + H2^ (M = Al, Ga)
Бескислородные соли образованы катионами металлов и амфигенов (а также катионом аммония NH4+) и анионами (остатками) бескислородных кислот; примеры: AgF, NaCl, KBr, PbI2, Na2S, Ba(HS)2, NaCN, NH4Cl. Проявляют некоторые химические свойства оксосолей.
Общий способ получения бескислородных солей с одноэлементными анионами – взаимодействие металлов и амфигенов с неметаллами F2, Cl2, Br2 и I2 (в общем виде Г2) и серой S (приведены реально протекающие реакции):
2М + Г2 = 2МГ (М = Li, Na, К, Rb, Cs, Ag)
M + Г2 = МГ2 (М = Be, Mg, Са, Sr, Ва, Zn, Mn, Со)
2М + ЗГ2 = 2МГ3 (М = Al, Ga, Cr)
2М + S = M2S (М = Li, Na, К, Rb, Cs, Ag)
M + S = MS (M = Be, Mg, Ca, Sr, Ba, Zn, Mn, Fe, Co, Ni)
2M + 3S = M2S3 (M = Al, Ga, Cr)
Исключения:
а) Cu и Ni реагируют только с галогенами Cl2 и Br2 (продукты МCl2, МBr2)
б) Cr и Mn реагируют с Cl2, Br2 и I2 (продукты CrCl3, CrBr3, CrI3 и MnCl2, MnBr2, MnI2)
в) Fe реагирует с F2 и Cl2 (продукты FeF3, FeCl3), с Br2 (смесь FeBr3 и FeBr2), с I2 (продукт FeI2)
г) Cu при реакции с S образует смесь продуктов Cu2S и CuS
Прочие бинарные соединения – все вещества этого класса, кроме выделенных в отдельные подклассы бескислородных кислот и солей.
Способы получения бинарных соединений этого подкласса разнообразны, самый простой – взаимодействие простых веществ (приведены реально протекающие реакции):
S + 3F2 = SF6, N2 + 3F2 = 2NF3
2P + 5Г2 = 2РГ5 (Г = F, CI, Br)
С + 2F2 = CF4
Si + 2Г2 = Sir4 (Г = F, CI, Br, I)
2As + 3S = As2S3
2E + 5S = E2S5 (E = P, As)
E + 2S = ES2 (E = C, Si)
3H2 + N2 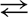 2NH3
2NH3
6M + N2 = 2M3N (M = Li, Na, K)
3M + N2 = M3N2 (M = Be, Mg, Ca)
2Al + N2 = 2AlN
3Si + 2N2 = Si3N4
2M + 2C = M2C2 (M = Li, Na)
2Be + С = Be2C
M + 2C = MC2 (M = Ca, Sr, Ba)
4Al + 3C = Al4C3
Si + С = SiC
4Li + Si = Li4Si
2M + Si = M2Si (M = Mg, Ca)
2M + H2 = 2MH (M = Li, Na, K)
M + H2 = MH2 (M = Mg, Ca)
2Na + O2 = Na2O2 (сгорание на воздухе)
M + O2 = МО2 (М = К, Rb, Cs; сгорание на воздухе)
Многие из этих веществ полностью реагируют с водой (чаще гидролизуются без изменения степеней окисления элементов, но гидриды выступают как восстановители, а надпероксиды вступают в реакции дисмутации):
РCl5 + 4Н2O = Н3РO4 + 5НCl
SiBr4 + 2Н2O = SiO2v + 4НBr
P2S5 + 8Н2O = 2Н3РO4 + 5H2S^
SiS2 + 2Н2O = SiO2v + 2H2S
Mg3N2 + 8H2O = 3Mg(OH)2v + 2(NH3 H2O)
Na3N + 4H2O = 3NaOH + NH3 H2O
Be2C + 4H2O = 2Be(OH)2v + CH4^
MC2 + 2H2O = M(OH)2 + C2H2^ (M = Ca, Sr, Ba)
Al4C3 + 12H2O = 4Al(OH)3v + 3CH4^
MH + H2O = MOH + H2^ (M = Li, Na, K)
MgH2 + 2H2O = Mg(OH)2v + H2^
CaH2 + 2H2O = Ca(OH)2 + H2^
Na2O2 + 2H2O = 2NaOH + H2O2
2MO2 + 2H2O = 2MOH + H2O2 + O2^ (M = K, Rb, Cs)
Другие вещества, наоборот, устойчивы по отношению к воде, среди них SF6, NF3, CF4, CS2, AlN, Si3N4, SiC, Li4Si, Mg2Si и Ca2Si.
1. Простые вещества – это
1) фуллерен
2) этилен
3) ацетон
4) озон
2. В формульных единицах продуктов реакций
Si + CF12 >…, Si + O2 >…, Si + Mg >…
общая сумма числа атомов всех элементов равна
1) 8
2) 9
3) 10

