окислителями. При растворении в воде дает бромную воду. Молекулы их также двухатомные, ковалентные неполярные, но они менее активны, чем фтор, что объясняется большим радиусом атома у брома и йода, чем у фтора. Все галогены – активные окислители, что проявляется при взаимодействии их с различными сложными веществами – смешивание сероводородной воды с раствором брома:
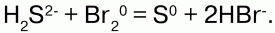
Бром с нулевой степенью окисления окисляет серу (-2) до 0, сам при этом восстанавливаясь до -1.
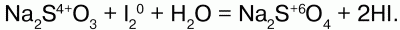
Галогены нашли широкое применение в химической промышленности: фтор используют в синтезе полимеров – фторопластов, пластмассы, стойкой к химическим воздействиям (тефлон), смазочных веществ, жидкостей для холодильников (фреоны). Бром используется в изготовлении лекарственных препаратов, некоторых красителей; йод широко используется в медицине – 10 %-ный раствор йода в спирте – как антисептическое, дезинфицирующее средство, йод входит в состав некоторых фармацевтических препаратов. Также бром и йод используются при различных синтезах и анализах веществ.
22. Общая характеристика подгруппы кислорода
Подгруппа кислорода, или халькогенов – 6-я группа периодической системы Д.И. Менделле-ва, включающая следующие элементы:
1) кислород – О;
2) сера – S;
3) селен – Se;
4) теллур – Te;
5) полоний – Po (радиоактивный элемент).
Номер группы указывает на максимальную валентность элементов, стоящих в этой группе. Общая электронная формула халькогенов: ns2np4– на внешнем валентном уровне у всех элементов имеется 6 электронов, которые редко отдают и чаще принимают 2 недостающих до завершения уровня электрона. Наличие одинакового валентного уровня обуславливает химическое сходство халькогенов. Характерные степени окисления: -1; -2; 0; +1; +2; +4; +6. Кислород проявляет только -1 – в пероксидах; -2 – в оксидах; 0 – в свободном состоянии; +1 и +2 – во фторидах – О2F2, ОF2 т. к. у него нет d-под-уровня и электроны разъединяться не могут, и валентность всегда – 2; S – все, кроме +1 и -1. У серы появляется d- подуровень и электроны с 3р и с 3s в возбужденном состоянии могут разъединиться и уйти на d-подуровень. В невозбужденном состоянии валентность серы – 2 – в SО, 4 – в SО2, 6 – в SО3. Se +2; +4; +6, Te +4; +6, Po +2; -2. Валентности у селена, теллура и полония также 2, 4, 6. Значения степеней окисления отражены в электронном строении элементов: О – 2s22p4; S – 3s23p4; Se – 4s24p4; Te – 5s25p4; Po – 6s26p4. Сверху вниз, с нарастанием внешнего энергетического уровня закономерно изменяются физические и химические свойства халькогенов: радиус атома элементов увеличивается, энергия ионизации и сродства к электрону, а также электроотрицательность уменьшаются; уменьшаются неметаллические свойства, металлические увеличиваются (кислород, сера, селен, теллур – неметаллы), у полония имеется металлический блеск и электропроводимость. Водородные соединения халькогенов соответствуют формуле: H2R: H2О, H2S, H2Sе, H2Те – хальководороды. Водород в этих соединениях может быть замещен на ионы металлов. Степень окисления всех халькогенов в соединении с водородом -2 и валентность тоже 2. При растворении хальководородов в воде образуются соответствующие кислоты. Эти кислоты – восстановители. Сила этих кислот сверху вниз возрастает, т. к. уменьшается энергия связи и способствует активной диссоциации. Кислородные соединения халькогенов отвечают формуле: RО2 и RО3 – кислотные оксиды. При растворении этих оксидов в воде они образуют соответствующие кислоты: Н2RО3 и Н2RO4. В направлении сверху вниз сила этих кислот убывает. Н2RО3 – кислоты-восстановители, Н2RO4 – окислители.
23. Кислород и его свойства
Кислород (О) стоит в 1 периоде, VI группе, в главной подгруппе. р- элемент. Электронная конфигурация 1s2
Физические свойства: кислород (О2) – бесцветный газ, без запаха и вкуса; в воде малорастворим, немного тяжелее воздуха. При -183 °C и 101,325 Па кислород сжижается, приобретая голубоватый цвет. Строение молекулы: молекула кислорода двухатомна, в обычных условиях прочная, обладает магнитными свойствами. Связь в молекуле ковалентная неполярная. Кислород имеет аллотропную модификацию – озон (О3) – более сильный окислитель, чем кислород.
Химические свойства: до завершения энергетического уровня кислороду нужно 2 электрона, которые он принимает проявляя степень окисления -2, но в соединении со фтором кислород ОF2 -2 и О2F2 -1. Благодаря химической активности кислород взаимодействует почти со всеми простыми веществами. С металлами образует оксиды и пероксиды:

Кислород не реагирует только с платиной. При повышенных и высоких температурах реагирует со многими неметаллами:


Непосредственно кислород не взаимодействует с галогенами. Кислород реагирует со многими сложными веществами:
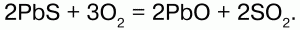
Кислороду характерны реакции горения:
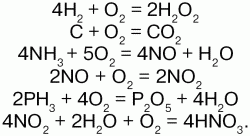
В кислороде горят многие органические вещества:
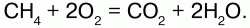
При окислении кислородом уксусного альдегида получают уксусную кислоту:
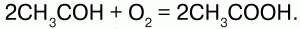
Получение: в лаборатории: 1) электролизом водного раствора щелочи: при этом на катоде выделяется водород, а на аноде – кислород; 2) разложением бертолетовой соли при нагревании: 2КСlО3?2КСl + 3О2?; 3) очень чистый кислород получают: 2КМnO4? К2МnO4 + МnО2 + О2?.
Нахождение в природе: кислород составляет 47,2 % массы земной коры. В свободном состоянии он содержится в атмосферном воздухе – 21 %. Входит в состав многих природных минералов, огромное его количество содержится в организмах растений и животных. Природный кислород состоит из 3 изотопов: О(16), О(17), О(18).
Применение: используется в химической, металлургической промышленности, в медицине.
24. Озон и его свойства
В твердом состоянии у кислорода зафиксировано три модификации: ?-, ?– и ?– модификации. Озон (О3) – одна из аллотропных модификаций кислорода. Строение молекулы: озон имеет нелинейное строение молекулы с углом между атомами 117°. Молекула озона обладает некоторой полярностью (несмотря на атомы одного рода, образующих молекулу озона), диамагнитна, так как не имеет неспаренных электронов.
Физические свойства: озон – синий газ, имеющий характерный запах; молекулярная масса = 48, температура плавления (твердого) = 192,7 °C, температура кипения = 111,9 °C. Жидкий и твердый озон взрывчат, токсичен, хорошо растворим в воде: при 0 °C в 100 объемах воды растворяется до 49 объемов озона.
Химические свойства: озон – сильный окислитель, он окисляет все металлы, в том числе золото – Au и платину – Pt (и металлы платиновой группы). Озон воздействует на блестящую серебряную пластинку, которая мгновенно покрывается черным пероксидом серебра – Аg2О2; бумага, смоченная скипидаром, воспламеняется, сернистые соединения металлов окисляются до солей серной кислоты; многие красящие вещества обесцвечиваются; разрушает органические вещества – при этом молекула озона отщепляет один атом кислорода, и озон превращается в обыкновенный кислород. Атакже большинство неметаллов, переводит низшие оксиды в высшие, а сульфиды их металлов – в их сульфаты:
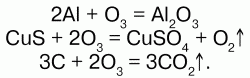
Йодид калия озон окисляет до молекулярного йода:
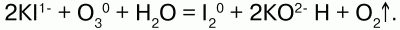
Но с пероксидом водорода Н2О2 озон выступает в качестве

